Marcia Brazuna1; Isabella Felix Q. Yamane2; Matheus A. P. Vieira1
DOI: 10.17545/eOftalmo/2025.0014
RESUMO
A atrofia macular extensa com pseudodrusas (EMAP) é uma maculopatia rara e progressiva, caracterizada por atrofia bilateral e simétrica de retina externa associada a depósitos tipo pseudodrusas e perda visual acentuada. Relata-se o caso de um paciente de 56 anos com diagnóstico de atrofia macular extensa com pseudodrusas, antecedente de glomerulonefrite pós-estreptocócica na infância e uso prolongado de penicilina benzatina. O paciente apresentava piora progressiva da acuidade visual e nictalopia há cinco anos, com acuidade final de 20/30 no olho direito e 20/400 no esquerdo. A tomografia de coerência óptica revelou pseudodrusas mais evidentes no polo posterior e separação focal entre o epitélio pigmentar da retina e a membrana de Bruch. A autofluorescência mostrou zonas hipoautofluorescentes bem delimitadas, e o eletrorretinograma evidenciou disfunção retiniana bilateral com predomínio de comprometimento cone-mediado, padrão descrito como o mais frequente na atrofia macular extensa com pseudodrusas. Os níveis séricos de C3, C4 e PCR estavam normais, sem sinais de inflamação sistêmica. Até onde sabemos, não há relatos prévios de EMAP em paciente com antecedente de glomerulonefrite pós-estreptocócica, achado que reforça a possibilidade de mecanismo imunoinflamatório da doença, embora sem relação causal demonstrada.
Palavras-chave: EMAP; Pseudodrusas; Complemento; Glomerulonefrite; Penicilina benzatina.
ABSTRACT
Extensive macular atrophy with pseudodrusen-like appearance is a rare, progressive maculopathy characterized by bilateral, symmetrical outer retinal atrophy, associated with pseudodrusen deposits and significant visual impairment. We report the case of a 56-year-old patient diagnosed with extensive macular atrophy with pseudodrusen-like appearance who had a history of childhood poststreptococcal glomerulonephritis and long-term exposure to benzathine penicillin. The patient presented with progressive visual acuity decline and nyctalopia over 5 yr, with a final best-corrected visual acuity of 20/30 in the right eye and 20/400 in the left eye. Optical coherence tomography demonstrated pseudodrusen deposits predominantly in the posterior pole as well as focal separation between the retinal pigment epithelium and Bruch's membrane. Fundus autofluorescence revealed sharply demarcated hypoautofluorescent areas, and full-field electroretinography showed bilateral cone-predominant dysfunction, the most frequently reported electrophysiologic pattern in extensive macular atrophy with pseudodrusen-like appearance. Serum complement C3 and C4 levels and C-reactive protein remained within normal limits, with no evidence of active systemic inflammation. To the best of our knowledge, this is the first report describing extensive macular atrophy with pseudodrusen-like appearance in a patient with a history of poststreptococcal glomerulonephritis, suggesting a possible immunoinflammatory association; however, current evidence does not support a causal relationship.
Keywords: EMAP; Pseudodrusen; Complement; glomerulonephritis; Benzathine penicillin
INTRODUÇÃO
A atrofia macular extensa com pseudodrusas (EMAP) é uma maculopatia rara, caracterizada por atrofia coriorretiniana bilateral, simétrica e de progressão acelerada, com perda visual tipicamente entre a quinta e a sexta década de vida1,2. Clinicamente, manifesta-se por nictalopia, escotomas centrais e periféricos e redução progressiva da acuidade visual. À fundoscopia, observa-se envolvimento macular predominante no eixo vertical, com depósitos do tipo pseudodrusas que se estendem à média periferia3-5.
Embora o fenótipo da EMAP seja distinto, é fundamental diferenciá-la da atrofia geográfica difusa da degeneração macular relacionada à idade (DMRI), particularmente da forma diffuse trickling, conhecida por sua evolução mais agressiva5. Para distinguir a EMAP de outras formas de atrofia macular, Antropoli et al.3 propuseram critérios diagnósticos que incluem atrofia bilateral e simétrica com bordas multilobuladas e orientação vertical; presença de pseudodrusas difusas; degeneração periférica tipo paving-stone; e achados característicos em exames multimodais. Na autofluorescência, destacam-se áreas hipoautofluorescentes bem definidas com bordas iso- a hiperautofluorescentes, e na tomografia de coerência óptica (OCT), a perda das camadas externas da retina, alterações do complexo epitélio pigmentar da retina (EPR)-membrana de Bruch e afinamento coroidal3,4,6. Alterações eletrofisiológicas com disfunção predominantemente cone-mediada complementam o diagnóstico funcional7,8.
Além dos achados estruturais, fatores ambientais e imunológicos têm sido implicados como cofatores de risco, incluindo exposição ocupacional e ativação persistente da cascata do complemento, sugerindo base imunoinflamatória modulada por mecanismos epigenéticos9-15. A investigação de fatores sistêmicos associados permanece relevante, especialmente diante de evidências emergentes de ativação imunológica crônica envolvendo vias do complemento, reforçando a importância de contextualizar casos com antecedentes inflamatórios ou infecciosos.
No contexto brasileiro, Moreira-Neto et al.16 relataram alta prevalência de febre reumática (90,9%) e uso prolongado de penicilina benzatina (94,8%) em pacientes com EMAP, levantando a hipótese de que a ativação imune mediada por infecção estreptocócica possa contribuir para o desenvolvimento da doença, e observaram que o uso do antibiótico é associado à menor extensão da atrofia, sugerindo possível efeito modulador ou protetor. O presente relato descreve um caso de EMAP em paciente com antecedente de glomerulonefrite pós-estreptocócica e uso prolongado de penicilina benzatina, associação não identificada na literatura consultada.
Esse caso é relevante por expandir as possíveis associações imunomediadas relacionadas à EMAP, reforçando a necessidade de investigação de antecedentes sistêmicos imunológicos em pacientes com achados compatíveis.
RELATO DO CASO
Paciente masculino, 56 anos, foi encaminhado para avaliação especializada devido à nictalopia e à piora progressiva da acuidade visual bilateral nos últimos cinco anos, mais acentuada em ambientes de baixa luminosidade. Negava dor ocular, metamorfopsias ou uso prévio de fármacos retinotóxicos. Fazia uso regular de óculos para correção de miopia e astigmatismo.
Como antecedentes pessoais, apresentava hipertensão arterial sistêmica, diabetes mellitus tipo 2 e infarto agudo do miocárdio prévio, todos controlados. Na infância, apresentou episódio de glomerulonefrite pós-estreptocócica, tratado com múltiplas aplicações de penicilina benzatina. Relatava ainda uso intermitente e prolongado do antibiótico na vida adulta, embora sem documentação precisa das indicações. Negava história familiar de doenças oculares hereditárias ou autoimunes.
A acuidade visual melhor corrigida era de 20/30 no olho direito e 20/400 no olho esquerdo. À biomicroscopia, observou-se catarata nuclear N2 em ambos os olhos. A fundoscopia revelou atrofia macular bilateral com padrão orientado verticalmente, irregularidades pigmentares e depósitos amarelados do tipo pseudodrusas predominantemente no polo posterior, associados à degeneração periférica tipo paving-stone (Figuras 1 e 2).
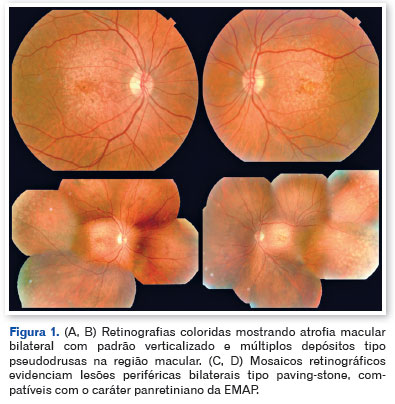
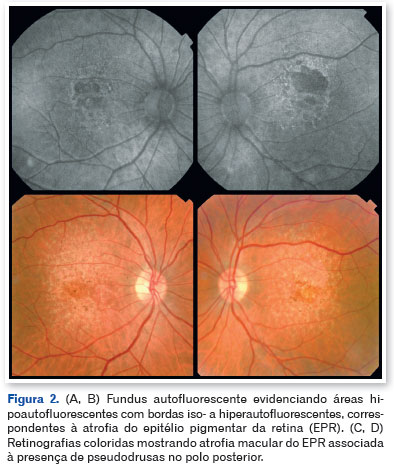
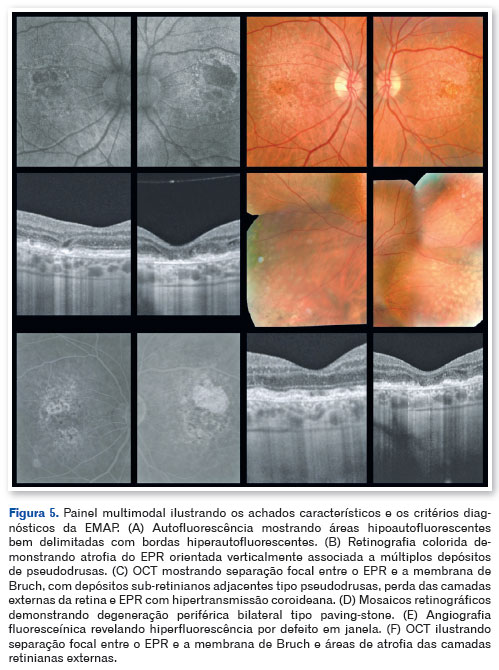
A tomografia de coerência óptica (OCT) mostrou pseudodrusas no polo posterior, separação focal entre o epitélio pigmentar da retina e a membrana de Bruch, além de áreas de atrofia macular. A autofluorescência evidenciou zonas hipoautofluorescentes bem delimitadas com bordas iso- a hiperautofluorescentes, compatíveis com perda do epitélio pigmentar da retina (Figuras 3, 4 e 5).
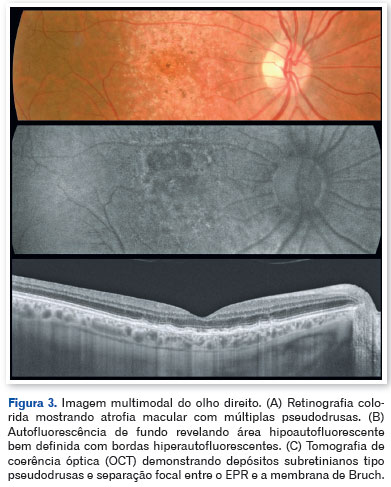
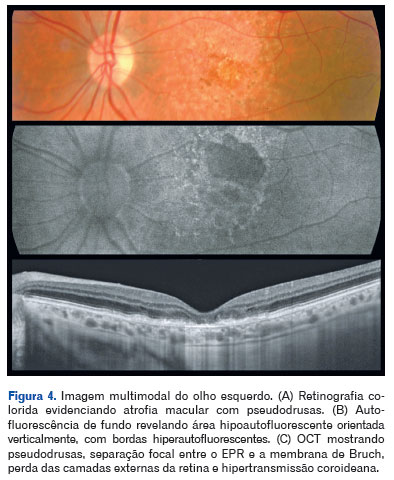
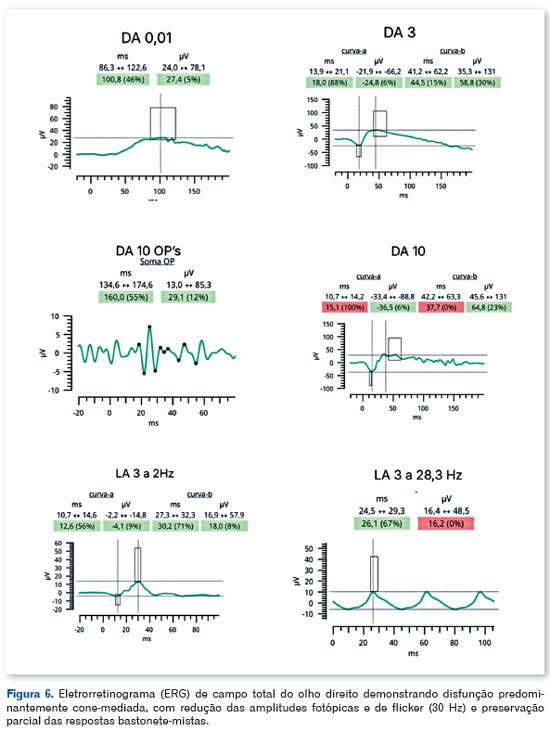
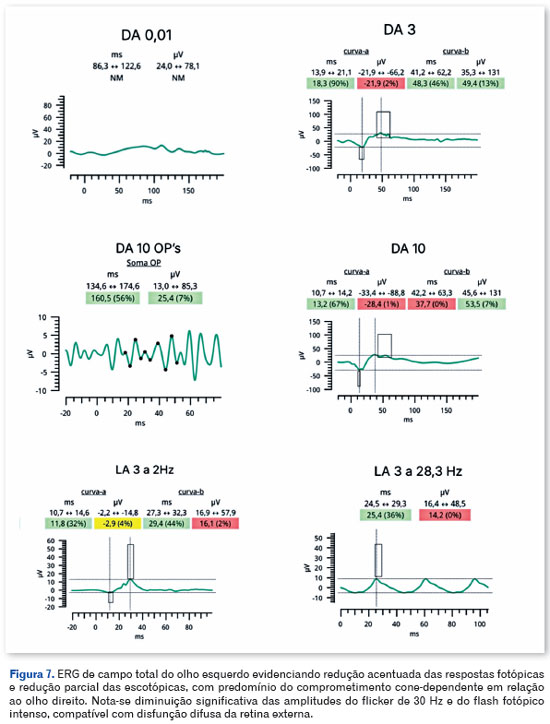
O eletrorretinograma (ERG) de campo total, realizado conforme protocolo ISCEV, demonstrou disfunção retiniana bilateral predominantemente cone-mediada, com redução das amplitudes fotópicas e de flicker (30 Hz) e preservação parcial das respostas bastonete-mistas, mais acentuada no olho esquerdo (Figuras 6 e 7).
Os exames laboratoriais mostraram níveis séricos normais de complemento (C3: 105 mg/dL; C4: 28,6 mg/dL) e marcadores inflamatórios dentro da normalidade (PCR: 0,1 mg/dL; VHS: 13 mm/h), afastando inflamação sistêmica ativa. Exames hematológicos e cardiovasculares não revelaram alterações relevantes.
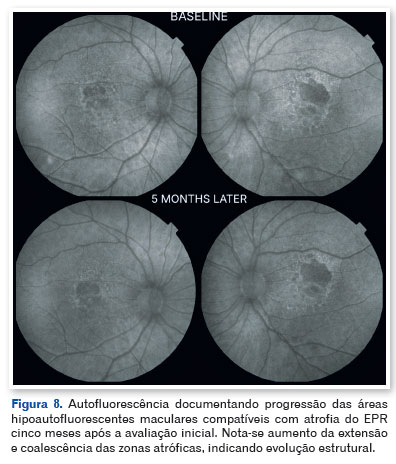
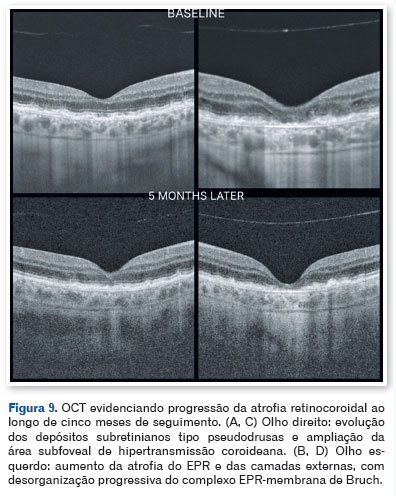
Com base nos achados clínicos e multimodais, estabeleceu-se o diagnóstico de Extensive Macular Atrophy with Pseudodrusen-like Appearance (EMAP). O paciente foi orientado quanto ao caráter degenerativo da doença e à importância do acompanhamento regular. Após cinco meses de seguimento, observou-se discreta progressão bilateral da atrofia, com piora funcional leve do olho esquerdo (Figuras 8 e 9).
DISCUSSÃO
O caso apresentado preenche os critérios clínicos e multimodais descritos para a EMAP, incluindo atrofia macular extensa bilateral e orientada verticalmente, presença de pseudodrusas e lesões periféricas do tipo paving-stone1-4,6. Desde a descrição inicial por Hamel et al.1, a EMAP tem sido reconhecida como entidade degenerativa distinta da degeneração macular relacionada à idade (DMRI) atrófica, devido à idade de início mais precoce e à progressão acelerada com envolvimento foveal2-4,17. Os achados estruturais deste caso reforçam o caráter panretiniano da doença.
O eletrorretinograma de campo total demonstrou disfunção retiniana bilateral predominantemente cone-mediada, com redução difusa das amplitudes fotópicas e de flicker e preservação parcial das respostas bastonete-mistas, corroborando disfunção difusa da retina externa e o caráter neurodegenerativo da EMAP7,8.
A fisiopatologia da EMAP ainda não está totalmente esclarecida, mas evidências indicam que a ativação anômala e sustentada da cascata do complemento desempenha papel central10,12,13. Essa ativação crônica e de baixo grau resulta em inflamação e perda progressiva das camadas externas da retina, culminando em atrofia retinocoroidal. Os mecanismos subjacentes, envolvendo resposta imune duradoura, parecem ser modulados por fatores genéticos e ambientais11,13,14. A ausência de alterações séricas detectáveis de C3, C4 e proteína C-reativa (PCR), como observada neste caso, não exclui a participação do complemento, uma vez que a ativação parece ocorrer predominantemente de forma local e subclínica. Evidências recentes sugerem que vias epigenéticas relacionadas à regulação do complemento e do controle inflamatório podem contribuir para a variabilidade fenotípica da doença10-13.
Um mecanismo de mimetismo molecular envolvendo antígenos estreptocócicos e proteínas retinianas tem sido hipotetizado como possível elo biológico entre infecções estreptocócicas prévias e degeneração retiniana imunomediada, apoiando a possibilidade de inflamação subclínica persistente com ativação crônica do complemento e dano cumulativo das estruturas retinocoroidais18,19.
Em estudo brasileiro, Moreira-Neto et al.16 relataram alta prevalência de febre reumática e uso prolongado de penicilina benzatina entre pacientes com EMAP, sugerindo que mecanismos imunes pós-estreptocócicos e possível imunomodulação crônica associada ao tratamento possam atuar como gatilhos imunológicos em indivíduos predispostos. De modo semelhante, Watanabe et al.7 demonstraram disfunção cone-mediada difusa, corroborando a amplitude do dano funcional descrito na EMAP.
Até o momento, não identificamos relatos na literatura que descrevam associação entre EMAP e glomerulonefrite pós-estreptocócica. Diferentemente das glomerulopatias mediadas pela via alternativa do complemento — como a nefropatia C3 e a doença por depósitos densos, nas quais a disfunção primária do complemento guarda relação mais direta com alterações retinianas — a glomerulonefrite pós-estreptocócica clássica é mediada predominantemente por imunocomplexos10,12,18. Ainda assim, a convergência entre ativação local do complemento, mecanismos de mimetismo molecular e predisposição imunológica pode sugerir uma via de interação imunobiológica, presente em indivíduos suscetíveis10,12,13,18.
A associação observada entre glomerulonefrite pós-estreptocócica e EMAP neste caso sugere possível vulnerabilidade imunológica compartilhada, embora sem evidência de relação causal. Este relato amplia o espectro de fatores sistêmicos potencialmente associados e reforça a plausibilidade de uma resposta autoimune crônica atuando como possível eixo comum entre manifestações sistêmicas e o fenótipo ocular da EMAP.
REFERÊNCIAS
1. Hamel CP, Meunier I, Arndt C, Ben Salah S, Lopez S, Bazalgette C, et al. Extensive macular atrophy with pseudodrusen-like appearance: a new clinical entity. Am J Ophthalmol. 2009;147(4): 609-20.
2. Carla MM, Giannuzzi F, Boselli F, Crincoli E, Rizzo S. Extensive macular atrophy with pseudodrusen-like appearance: comprehensive review of the literature. Graefes Arch Clin Exp Ophthalmol. 2024;262(10):3085-97.
3. Antropoli A, Bianco L, Romano F, Trinco A, Arrigo A, Benadji A, et al. Extensive macular atrophy with pseudodrusen-like appearance (EMAP): clinical characteristics, diagnostic criteria, and insights from allied inherited retinal diseases and age-related macular degeneration. Prog Retin Eye Res. 2025;104:101320.
4. Antropoli A, Bianco L, Condroyer C, Antonio A, Navarro J, D'Agostino D, et al. Extensive macular atrophy with pseudodrusen-like appearance: progression kinetics and late-stage findings. Ophthalmology. 2024;131(10):1175-84.
5. Antropoli A, Arrigo A, Bianco L, Berni A, Lamberto F, Saladino A, et al. Quantitative multimodal imaging of extensive macular atrophy with pseudodrusen and geographic atrophy with diffuse trickling pattern. Sci Rep. 2023;13(1):1822.
6. Battaglia Parodi M, Antropoli A, Bianco L, Arrigo A, Pili L, Saladino A, et al. Peripheral retinal involvement in extensive macular atrophy with pseudodrusen-like deposits. Ophthalmol Retina. 2023;7(10):910-7.
7. Watanabe SES, Quercia AZF, Sacai PY. Electrophysiological findings in extensive macular atrophy with pseudodrusen. Doc Ophthalmol. 2023;147(2):121-30.
8. Robson AG, Frishman LJ, Grigg J, Hamilton R, Jeffrey BG, Kondo M, et al. ISCEV Standard for full-field clinical electroretinography (2022 update). Doc Ophthalmol. 2022;144(3):165-77.
9. Spaide RF, Vavvas DG. Complement inhibition for geographic atrophy: review of salient functional outcomes and perspective. Retina. 2023;43(7):1064-9.
10. Morgan BP, Harris CL. Complement, a target for therapy in inflammatory and degenerative diseases. Nat Rev Drug Discov. 2015;14(12):857-77.
11. Lambert NG, ElShelmani H, Singh MK, Mansergh FC, Wride MA, Padilla M, et al. Risk factors and biomarkers of age-related macular degeneration. Prog Retin Eye Res. 2016;54:64-102.
12. Armento A, Ueffing M, Clark SJ. The complement system in age-related macular degeneration. Cell Mol Life Sci. 2021;78(10): 4487-505.
13. Adamus G. Importance of autoimmune responses in progression of retinal degeneration initiated by gene mutations. Front Med (Lausanne). 2021;8:672444.
14. Douillard A, Picot MC, Delcourt C, Defoort-Dhellemmes S, Marzouka NA, Lacroux A, et al. Dietary, environmental, and genetic risk factors of extensive macular atrophy with pseudodrusen: a severe bilateral macular atrophy of middle-aged patients. Sci Rep. 2018;8(1):6840.
15. Douillard A, Picot MC, Delcourt C, Lacroux A, Zanlonghi X, Puech B, et al. Clinical characteristics and risk factors of extensive macular atrophy with pseudodrusen: the EMAP case-control national clinical trial. Ophthalmology. 2016;123(9):1865-73.
16. Moreira-Neto CA, Schmidt Andujar RA, Chao JCT, Vasconcelos H, Alves FEE, Rodrigues GD, et al. Rheumatic fever and long-term use of benzathine penicillin as possible risk factors for extensive macular atrophy with pseudodrusen in a Brazilian cohort. Int J Retina Vitreous. 2024;10(1):75.
17. Romano F, Cozzi M, Monteduro D, Oldani M, Boon CJF, Staurenghi G, et al. Natural course and classification of extensive macular atrophy with pseudodrusen-like appearance. Retina. 2023;43(3):402-11.
18. Cunningham MW. Molecular mimicry, autoimmunity, and infection: the cross-reactive antigens of group A streptococci and their sequelae. Microbiol Spectr. 2019;7(4).
19. Lerner MP, Donoso LA, Nordquist RE, Cunningham MW. Immunological mimicry between retinal S-antigen and group A streptococcal M proteins. Autoimmunity. 1995;22(2):95-106.
| INFORMAÇÕES DOS AUTORES |
|
 |
» Marcia Brazuna https://orcid.org/0009-0008-0688-8596 http://lattes.cnpq.br/9692116316379230 |
 |
» Matheus A. P. Vieira https://orcid.org/0009-0002-8178-7978 http://lattes.cnpq.br/3913686891761563 |
 |
» Isabella Felix Q. Yamane https://orcid.org/0009-0001-3418-8596 http://lattes.cnpq.br/0474957487960468 |
Financiamento: Declaram não haver.
Conflitos de Interesse: Declaram não haver.
Recebido em:
10 de Janeiro de 2025.
Aceito em:
24 de Setembro de 2025.